اتانول
اتانول چیست؟
اتانول یک حلال جهانی در نظر گرفته می شود، زیرا ساختار مولکولی آن اجازه می دهد تا هر دو قطب، آب دوست و غیر قطبی، ترکیبات آبگریز حل شود. در واقع اتانول نوعی الکل و یک ترکیب شیمیایی آلی است.
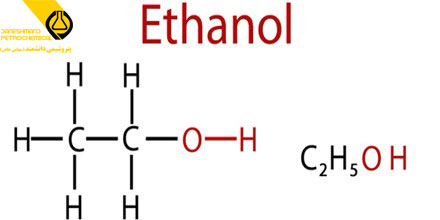
این الکل ساده دارای فرمول شیمیایی C₂H₆O است. فرمول آن را می توان به صورت CH₃−CH₂−OH یا C₂H₅OH نیز نوشت، و غالباً به اختصار EtOH نامیده می شود. اتانول مایعی فرار، قابل اشتعال و بی رنگ است که دارای بوی مشخص کمی است. اتانول به طور طبیعی با تخمیر قندها توسط مخمرها یا از طریق فرآیندهای پتروشیمی مانند هیدراتاسیون اتیلن، تولید می شود.
این به عنوان ضد عفونی کننده کاربردهای پزشکی دارد. به عنوان یک حلال شیمیایی و در ترکیب ترکیبات آلی استفاده می شود. اتانول یک منبع سوخت جایگزین است و یک حلال همه کاره است، که با آب و بسیاری از حلال های آلی مخلوط می شود.
اتانول مایعی فرار و بی رنگ است که بوی کمی دارد. با شعله آبی بدون دود می سوزد که همیشه در نور طبیعی قابل مشاهده نیست. خصوصیات فیزیکی اتانول اساساً از وجود گروه هیدروکسیل و کوتاه بودن زنجیره کربن آن ناشی می شود. گروه هیدروکسیل اتانول قادر به شرکت در پیوند هیدروژن است و باعث چسبندگی و فرار شدن آن نسبت به ترکیبات آلی قطبی کمتر با وزن مولکولی مشابه مانند پروپان می شود.
تاریخچه اتانول:
از دوران پیش از تاریخ توسط انسان به عنوان ماده مست کننده نوشیدنی های الکلی از اتانول استفاده می شده است. باقی مانده های خشک شده سفال های 9000 ساله که در شمال سرزمین اصلی چین یافت شده است، حاکی از استفاده از مشروبات الکلی حتی در میان مردم نوسنگی است. انزوای آن به عنوان یک ترکیب نسبتاً خالص ابتدا توسط کیمیاگران پارسی حاصل شد که در دوران خلافت عباسی هنر تقطیر را توسعه دادند، که مشهورترین آن ها الرضی بود.
با تقطیر اتانول از آب محصولی حاصل می شود که حداکثر 6/95 درصد اتانول باشد، زیرا اتانول با آب یک آزوتروپ تشکیل می دهد. اتانول مطلق اولین بار در سال 1796 توسط یوهان توبیاس لوویتز، با فیلتر کردن اتانول مقطر از طریق ذغال به دست آمد.
اتانول برای اولین بار به طور مصنوعی و در سال 1826، با تلاش مستقل هنری هنل در بریتانیا در فرانسه تهیه شد. مایکل فارادی با هیدراتاسیون اسید کاتالیزور اتیلن در سال 1828، فرآیندی مشابه فرآیند تولید سنتز اتانول صنعتی، اتانول را تهیه کرد.
جدول مشخصات فنی اتانول:
| نام آیوپاک | اتانول |
| جرم مولکولی اتانول | 46.07 g/mol |
| فرمول شیمیایی اتانول | C2H5OH |
| نقطه جوش | 173.1°F – 78.37°C |
| چگالی | 0.789 g/cm3 |
| نقطه ذوب | -173.5°F |
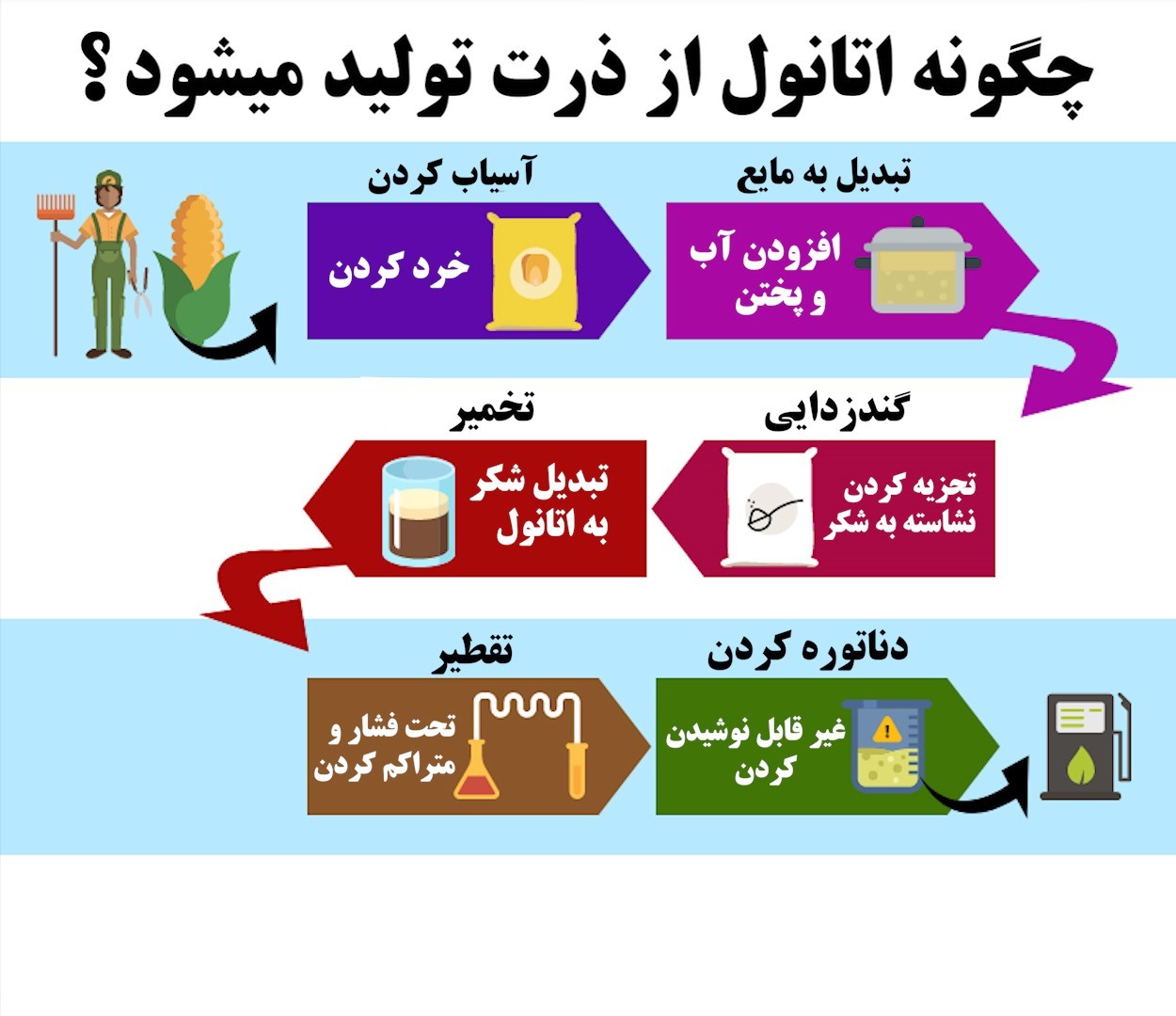
تولید اتانول:
روش تولید اتانول به نوع ماده اولیه مصرفی بستگی دارد. این فرآیند برای مواد غذایی نشاسته ای یا پایه شکر کوتاهتر از مواد اولیه سلولزی است. تولید اتانول مبتنی بر نشاسته و قند است.
اتانول یک سوخت جایگزین تولید داخل است که معمولاً از ذرت، گندم یا چغندر ساخته می شود. این ماده همچنین از مواد اولیه سلولزی مانند بقایای محصول و چوب نیز ساخته می شود. اگرچه این مورد معمول نیست.
آسیاب خشک فرآیندی است که ذرت را به آرد خرد کرده و با محصولات مشترک از غلات مقطر و دی اکسید کربن، آن را به اتانول تخمیر می کند.
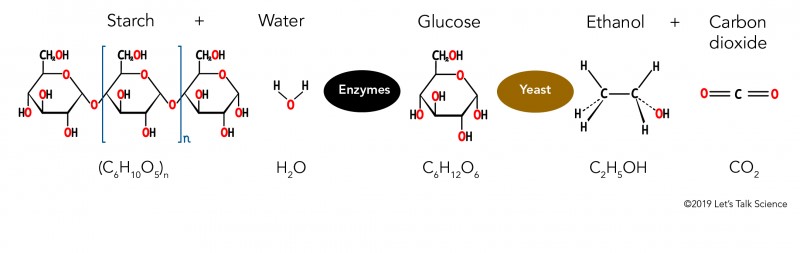
تولید اتانول از مواد خوراکی سلولزی: مانند علف، چوب و بقایای محصولات یک فرآیند درگیرتر از استفاده از محصولات پایه نشاسته ای است. دو مسیر اصلی برای تولید اتانول سلولزی وجود دارد: بیوشیمیایی و ترموشیمیایی. روند بیوشیمیایی شامل یک پیش تصفیه برای آزاد سازی قندهای هم سلولز و به دنبال آن هیدرولیز برای تجزیه سلولز به قندها است. قندها به اتانول تخمیر می شوند و لیگنین بازیابی می شود و برای تولید انرژی برای تولید فرآیند مورد استفاده قرار می گیرد. فرآیند تبدیل ترموشیمیایی شامل افزودن گرما و مواد شیمیایی به یک ماده اولیه زیست توده برای تولید سینگاس است که مخلوطی از مونوکسیدکربن و هیدروژن است. سینگاس با کاتالیزور مخلوط شده و به اتانول و سایر محصولات مایع تبدیل می شود.
اتانول هم به صورت پتروشیمی، هم از طریق هیدراتاسیون اتیلن و هم از طریق فرآیندهای بیولوژیکی، با تخمیر قندها با مخمر تولید می شود. اینکه کدام فرآیند از نظر اقتصادی مقرون به صرفه تر است، به قیمت های غنی از ذخایر خوراک نفت و غلات بستگی دارد.
ساختار اتانول:
در اتانول دو نوع پیوند وجود دارد. پیوندهای CH کووالانسی غیر قطبی هستند، زیرا این اتم ها از نظر الکترونگاتیوی مشابه هستند (توانایی یک اتم در جذب الکترون به خود هنگامی که به یک اتم دیگر در یک ترکیب متصل شود.) پیوندهای CO و OH کووالانسی قطبی هستند، زیرا O به طور قابل توجهی بیشتر است منفی الکتریکی از C یا H. از این رو یک بار + کمی (d +) در C و H متصل به O و یک بار کم (d-) در O وجود دارد.
بار رسمی هر اتم در اتانول صفر است. این با اختصاص الکترون به هر اتم در اتانول و مقایسه عدد اختصاص داده شده به هر اتم با تعداد یافت شده در پوسته خارجی اتم منفصل نشده محاسبه می شود. جفت های تنها به اتمی که در ساختار لوئیس قرار گرفته اند، اختصاص داده شده اند. الکترون های پیوندی به طور مساوی بین دو اتم پیوند تقسیم می شوند. اگر به اتم موجود در یک مولکول تعداد الکترون هایی بیشتر از اتم های تنها در پوسته خارجی خود اختصاص داده شود، بار منفی آن برابر با تعداد اضافی الکترون خواهد بود. بارهای مثبت وقتی کمتر به آن ها اختصاص می یابد، رشد می کنند.
با داشتن 8 الکترون (4 جفت) C و O اتانول، هندسه ابرهای الکترون در اطراف C و O چهار ضلعی است و زاویه پیوند آنها تقریباً 109 درجه است. در این آرایش، ابرهای الکترون که یکدیگر را دفع می کنند، تا حد ممکن از هم دور هستند. از آنجا که 4 اتم به هر کربن متصل است، هندسه اتم های اطراف C نیز چهار وجهی است. با این حال، فقط دو اتم (C و H) به O متصل هستند، بنابراین هندسه اتم های اطراف O خم یا زاویه دار است. این هندسه نشان می دهد که آن ها جدایی از مرکز مثبت و کمی منفی در مولکول هستند، که این قطب را قطبی می کند.
اتانول یک ترکیب یونی است یا مولکولی؟
محلول های آبی نوعی محلول است که در آن حلال، آب می باشد. معمولاً بعد از ترکیب به عنوان (aq) برچسب گذاری می شود. به عنوان مثال (NaCl)aq این همچنین به معنای حل شدن املاح در آب است. انواع محلول های آبی وجود دارد: یونی و مولکولی. محلول آبی یونی وقتی است که املاح یک ترکیب یونی باشد یا در داخل محلول به یون ها تقسیم شود. از طرف دیگر مولکولی در یون ها در محلول جدا نمی شود. اتانول یا C2H6O وقتی در محلول است، یون تشکیل نمی دهد. بنابراین ترکیب مولکولی است.
اتانول خوراکی:
الکل ها، به اشکال مختلف، در داروها به عنوان ضد عفونی کننده، و پادزهر استفاده می شوند. انواع الکل مورد استفاده شامل اتانول، اتانول دناتوره شده، 1-پروپانول و الکل ایزوپروپیل است. الکل ها در برابر طیف وسیعی از میکروارگانیسم ها موثر هستند، اگرچه اسپورها را غیرفعال نمی کنند. غلظت های 60 تا 90٪ بهترین نتیجه را دارند.
الکل خوراکی یا اتانول به عنوان ضد عفونی کننده از اوایل سال 1363 مورد استفاده قرار گرفته است، شواهدی برای حمایت از استفاده از آن در اواخر دهه 1800 موجود است. این دارو در فهرست داروهای ضروری سازمان بهداشت جهانی قرار دارد. فرمولاسیون های تجاری مالش الکلی مبتنی بر الکل یا با عوامل دیگر مانند کلرهگزیدین در دسترس است.
مصارف پزشکی اتانول:
از الكل های خوراکی برای ضد عفونی كردن پوست قبل از چوب سوزن و قبل از جراحی استفاده می شود. این مواد ممکن است برای ضد عفونی کننده پوست و دستان ارائه دهنده خدمات بهداشتی مورد استفاده قرار گیرند. همچنین می توان از آن ها برای تمیز کردن مناطق دیگر و در دهان شویه ها استفاده کرد. از طریق دهان یا تزریق داخل ورید، از اتانول برای درمان سمیت متانول یا اتیلن گلیکول در صورت عدم وجود فومپیزول نیز استفاده می شود.
مسمومیت با متانول:
در صورت عدم استفاده از فومپیزول، از طریق دهان یا تزریق داخل ورید از اتانول برای درمان سمیت متانول یا اتیلن گلیکول استفاده می شود.
اتانول، هنگامی که برای سمیت استفاده می شود، با الکل های دیگر برای آنزیم الکل دهیدروژناز، کاهش متابولیسم به آلدئید سمی و مشتقات اسید کربوکسیلیک و کاهش اثر سمی جدی گلیکول ها برای تبلور در کلیه ها رقابت می کند.
حلالیت اتانول:
پیوند هیدروژنی باعث می شود اتانول خالص به همان اندازه رطوبت ساز باشد که به راحتی آب را از هوا جذب کند. ماهیت قطبی گروه هیدروکسیل باعث می شود که اتانول بسیاری از ترکیبات یونی، به ویژه هیدروکسیدهای سدیم و پتاسیم، کلرید منیزیم، کلرید کلسیم، کلرید آمونیوم، برومید آمونیوم و برومید سدیم را حل کند. کلریدهای سدیم و پتاسیم در اتانول کمی محلول هستند. از آنجا که انتهای مولکول اتانول نیز غیر قطبی است، مواد غیر قطبی از جمله اکثر روغن های اساسی و بسیاری از مواد طعم دهنده، رنگی و دارویی را حل می کند.
تفاوت اتانول با سایر الکل های بلند زنجیر در اختلاط پذیری اتانول با آب است. اتانول با آب کاملا مخلوط می شود در حالی که الکل های با زنجیر طولانی تر (پنج یا بیشتر از اتم های کربن) در آب حل نمی شوند. در واقع با افزایش تعداد کربن ها در الکل های بلند زنجیر، میزان اختلاط آب آن ها به شدت کاهش می یابد.
علاوه بر مواد قطبی، مواد غیر قطبی در اتانول حل می شوند، مولکول اتانول دارای یک گروه دوستدار آب (آب دوست) -OH است که به آن کمک می کند تا مولکول های قطبی و مواد یونی را حل کند. زنجیره هیدروکربن کوتاه و ترسناک از آب (آبگریز) CH3CH2– می تواند مولکول های غیر قطبی را جذب کند. بنابراین اتانول می تواند مواد قطبی و غیر قطبی را حل کند.
کاربرد اتانول:
- اتانول به عنوان یک داروی کاهش دهنده سیستم عصبی مرکزی، یکی از داروهای روانگردان است که بیشتر مورد مصرف قرار می گیرد.
- بیشترین استفاده از اتانول به عنوان سوخت موتور و مواد افزودنی سوخت.
- از اتانول به عنوان سوخت موشک استفاده شده است و در حال حاضر در هواپیماهای سبک وزن موشکی مسابقه ای است.
- اتانول به دلیل در دسترس بودن گسترده، هزینه کم، خلوص بالا و سمیت کم، در پیل های سوختی استفاده می شود.
- در سیستم های گرمایش خانگی مانند شومینه های اتانولی می توان برای گرم کردن خانه یا تزئینات نیز از آن استفاده کرد.
- در ساخت و تولید مواد اولیه و به عنوان پیش ماده برای سایر ترکیبات آلی مانند اتیل هالیدها، استرهای اتیل، اتیل اتر، استیک اسید و آمین های اتیل کاربرد گسترده ای دارد.
- به عنوان یک حلال پس از پردازش برای از بین بردن روغن ها، موم ها و کلروفیل از محلول در فرایندی که به عنوان زمستان زدایی استفاده می شود.
- اتانول در رنگ ها، تنتورها، مارکرها و محصولات مراقبت شخصی مانند دهان شویه ها، عطرها و دئودورانت ها وجود دارد.
- پلی ساکاریدها از محلول آبی در حضور الکل رسوب می کنند و به همین دلیل در تصفیه DNA و RNA از رسوب اتانول استفاده می شود.
- از اتانول بعلت نقطه انجماد کم وسمیت کم، بعضاً در آزمایشگاه ها با یخ خشک یا سایر مواد خنک کننده به عنوان حمام خنک کننده استفاده می شود، تا ظرف ها را در دمای پایین تر از نقطه انجماد آب نگه دارد. به همین دلیل، از آن به عنوان مایع فعال در دماسنج های الکلی نیز استفاده می شود.
- کاربرد اصلی آن به عنوان حلال در تهیه تنتور ید، شربت های سرفه و غیره است. همچنین با هیدروکربن های آلیفاتیک سبک مانند پنتان و هگزان و کلریدهای آلیفاتیک مانند تری کلرواتان و تتراکلر اتیلن قابل اختلاط است.
- تولید یخ خشک (CO2 منجمد) برای استفاده در ذخیره سازی سرما
- حمایت از فتوسنتز در گلخانه های گیاهی
لیست قیمت اتانول:
| ردیف | نام محصول | قیمت |
| 1 | قیمت اتانول طبی 96% | تماس بگیرید |
| 2 | قیمت اتانول خوراکی 70% | تماس بگیرید |





سلام. خیلی آموزنده و عالی.
این همون الکی است ک باهاش مردم خفه میکنند؟!
با سلام
خیر
عالی بود
خیلی مفید