خرید بی کربنات سدیم | 5 نکته طلایی انتخاب و استفاده
به همراه نمونه رایگان جهت تست
بی کربنات سدیم به عنوان جوش شیرین، بی کربنات سودا و یا سدیم هیدروژن کربنات نیز شناخته می شود، یک ترکیب شیمیایی با فرمول NaHCO3 می باشد. این نمک از کاتیون سدیم (+Na) و آنیون بی کربنات (–HCO3) تشکیل شده است. نمک بی کربنات سدیم در آب، به سدیم و بی کربنات تجزیه می شود.
این تجزیه یک محلول را قلیایی می کند، به این معنا که قادر است اسید را خنثی کند. به همین دلیل، این ماده اغلب برای درمان بیماری های ناشی از اسیدیته بالا در بدن مانند سوزش معده استفاده می شود. به منظور خرید بی کربنات سدیم و خرید جوش شیرین با کارشناسان فروش پتروشیمی دانشمند تماس حاصل فرمائید.
جالب است که بدانید که جوش شیرین از ترکیب سودا اش سبک با مولکول های آب اضافی تولید شده و به طور وسیعی در صنایع تولیدی مواد شوینده و صابون ها مورد استفاده قرار می گیرند، تا خاصیت شویندگی آن ها را تا حد قابل زیادی افزایش دهد.
~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
🔴امکان ارسال این محصول به سراسر کشور در کمتر از ۷ روز، با قیمت مناسب و بدون واسطه فراهم است🔴
🔸 برای دریافت اطلاعات بیشتر و استعلام قیمت، لطفاً در تماس باشید 🔸
~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
بی کربنات سدیم چیست؟
یک جامد سفید بلوری است، اما اغلب به صورت یک پودر خوب ظاهر می شود. طعم کمی شور و قلیایی شبیه طعم جوش شیرین دارد. شکل معدنی طبیعی آن ناکولیت است. این ترکیب در میان ترکیبات سدیم، یکی از موادی است که کمترین قلیائیت را دارد. این جز component ماده معدنی نترون است و در بسیاری از چشمه های معدنی محلول یافت می شود. بی کربنات سودا در دمای اتاق، به فرم جامد است. حلالیت یا توانایی حل شدن ماده در آب نیز از دیگر ویژگی های فیزیکی این ماده است و در آب محلول است و می تواند از طریق تبخیر از آب جدا شود.
محلول مولار 1 درصد مولد جوش شیرین در آب در دمای اتاق دارای pH برابر 8.3 است. این عدد نشان دهنده قلیایی بودن جوش شیرین است که مزه تلخ آن را به خود اختصاص می دهد.
جوش شیرین چیست؟
جوش شیرین یک عامل خمیرمایه است و در واقع یک پودر کریستالی سفید است که به طور طبیعی قلیایی یا پایه است. جوش شیرین هنگامی فعال می شود که با مواد مایع و اسیدی ترکیب شود. با فعال شدن، دی اکسید کربن تولید می شود که اجازه می دهد کالاهای پخته شده بلند شوند و سبک و کرکی شوند. جوش شیرین را با فرمول شیمیایی NaHCO3 می شناسند، که در کالاهای پخته شده مانند کیک، کلوچه استفاده می شود.

تجزیه بی کربنات سدیم:
تجزیه فرآیندی است که با استفاده از گرما تجزیه یک ماده به اجزای ساده تر و متفاوت از ماده اصلی انجام می شود. هنگامی که تا دمای بالاتر از 50 درجه سانتیگراد (122 درجه فارنهایت) گرم می شود، بی کربنات سدیم تجزیه می شود یا از هم جدا می شود و بیشتر دی اکسید کربن (CO2) و آب (H2O) با مقادیر کمی کربنات سدیم (NaCO3) تشکیل می دهد. تجزیه یک تغییر شیمیایی است.
جدول مشخصات فنی جوش شیرین:
| فرمول شیمیایی | NaHCO3 |
| شکل ظاهری | بلور سفید |
| pH | 8.5 |
| جرم مولی |
84.0066 g/mol |
| نقطه ذوب |
50 °C |
| نقطه جوش |
851 °C |
| حلالیت | محلول در آب، در اتانول نامحلول و در متانول و استون کمی محلول است. |
| آنتروپی مولار |
102 J/mol⋅K |
| دانسیته |
2.2 g/cm³ |
| نام آیوپاک | Sodium hydrogen carbonate |
تاریخچه بی کربنات سودا یا جوش شیرین:
هزاران سال است که مردم از جوش شیرین استفاده می کنند. مصریان باستان از رسوبات طبیعی این ماده معدنی برای تمیز کردن دندان های خود و ساختن رنگ برای نوشتن استفاده می کردند. در دهه 1830، نانوایان نیویورک برای تهیه نان شروع به افزودن این ماده و شیر ترش به خمیر کردند.
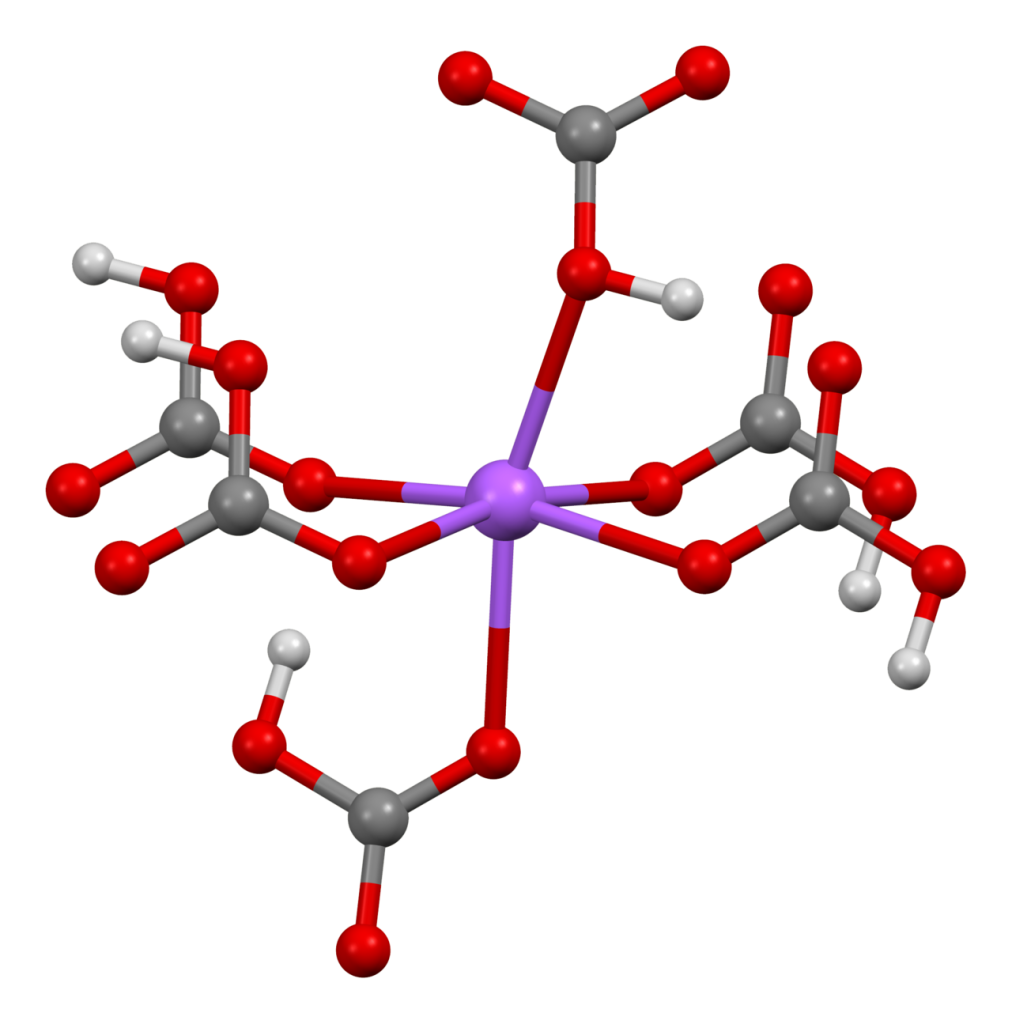
ساختار بی کربنات سدیم:
این ترکیب از اختلاط مولکول های کربن، سدیم، هیدروژن و اکسیژن تشکیل می شود. این مخلوط که به جوش شیرین نیز معروف است، در واقع نوعی نمک است.
واکنش های شیمیایی جوش شیرین:
1. بی کربنات سودا یک ترکیب آمفوتریک است. محلول های آبی به دلیل تشکیل اسید کربنیک و یون هیدروکسید ملایم قلیایی هستند. بی کربنات سودا می تواند به عنوان شستشو دهنده برای از بین بردن هرگونه ناخالصی های اسیدی از مایع خالص و تولید نمونه خالص تر استفاده شود. واکنش بی کربنات سدیم و یک اسید نمک و اسید کربنیک تولید می کند، که به راحتی به دی اکسید کربن و آب تجزیه می شود:
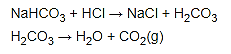
2. با اسید استیک (موجود در سرکه) واکنش می دهد و استات سدیم، آب و دی اکسید کربن تولید می کند:
![]()
3. با بازهایی مانند هیدروکسید سدیم واکنش داده و کربنات ها را تشکیل می دهد:
![]()
کاربرد ها و موارد مصرف بی کربنات سدیم (جوش شیرین)
1. در پخت و تهیه غذا
جوش شیرین موجود در فروشگاه های مواد غذایی بی کربنات سودا خالص و دارای درجه غذایی است. نانوایان مقدار کمی جوش شیرین را به مخلوط آرد، شکر، تخم مرغ، کره و سایر مواد موجود در کیک ها، کلوچه ها و سایر محصولات پخته شده اضافه می کنند.

از جوش شیرین همراه با مایه ترشی که اسیدی است، استفاده می شود و محصول سبک تری با طعم اسیدی کمتری تولید می شود. بسیاری از بوهای بد ناشی از اسیدها هستند و جوش شیرین هنگام واکنش با آن ها، این بوها را خنثی می کند. گازی که در طی واکنش اسید و باز بین جوش شیرین و اسیدی مانند خامه تارتار، آب لیمو یا اسید لاکتیک در دوغ آزاد می شود، باعث بالا رفتن کالاهای پخته می شود.
2. محصولات مراقبت شخصی و داروها
در محصولات مراقبت از پوست و مراقبت های شخصی مانند لوسیون ها و نمک های حمام، جوش شیرین به کنترل تعادل اسید و باز محصول برای جلوگیری از خراب شدن آن کمک می کند. در خمیر دندان، بی کربنات سدیم یا جوش شیرین با جدا کردن ذرات ریز غذا یا نوشیدنی هایی که می توانند مینای دندان را لکه دار کنند، به از بین بردن لکه های دندان کمک می کند.

همچنین یک ماده رایج در دئودورانت است، زیرا می تواند به خنثی سازی رایحه های اسیدی بد بو کمک کند. سدیم هیدروژن کربنات همچنین ماده موثری در محصولات ضد اسیدی است که برای تسکین دل درد و معالجه سو هاضمه اسید استفاده می شود. این کار با خنثی سازی سریع اسید معده و تسکین موقتی علائم ریفلاکس اسید انجام می شود.
3. شوینده ها و حلال ها
سدیم هیدروژن کربنات یک ماده رایج در تمیز کردن، شوینده و چربی زدایی محصولات است. در محصولات تمیز کردن، این ماده می تواند با سرکه واکنش دهد و محلولی ایجاد کند که به تخلیه زهکشی یا از بین بردن جرم در کوره کمک می کند. سایشی جزئی آن برای از بین بردن بقایای سوخته یا چربی بسیار کارآمد است.
4. احتراق
از سدیم هیدروژن کربنات همچنین برای تأخیر در واکنش های احتراق با آزاد سازی CO2 و H2O در هنگام گرم شدن استفاده می شود، که هر دو بازدارنده شعله هستند.
5. کاربردهای سدیم هیدروژن کربنات در صنعت
- به عنوان کنترل آفات برای از بین بردن سوسک ها و کنترل رشد قارچ ها استفاده می شود.
- به عنوان ضد عفونی کننده استفاده می شود.
- برای محافظت از زیر بغل از بوی بد و تحریک استفاده می شود.
- از آن در آشپزی به ویژه برای پخت مواد غذایی استفاده می شود.
- به عنوان یک ماده برای ساخت دارو به منظور تزریق وریدی برای جلوگیری از عوارض جانبی شیمی درمانی استفاده می شود.
- به دلیل خاصیت ضد باکتری بودن برای شستشوی محصولات آشپزخانه استفاده می شود.
- برای تمیز بودن دندان و دهان استفاده می شود.
- در مصرف عامه، به منظور سفید کنندگی و تمیز کنندگی پارچه در خشک شویی ها استفاده می شود.

- 25 درصد از مقدار کل سدیم هیدروژن کربنات مورد استفاده در سراسر جهان به عنوان افزودنی خوراک دام استفاده می شود.
- در صنعت نساجی برای رنگرزی پشم، ابریشم و چرم از بی کربنات سدیم استفاده می کنند.
- در تولید پلاستیک و پلیمرهای پیچیده از جوش شیرین به عنوان تصفیه کننده و کاتالیزور استفاده می کنند.
آیا جوش شیرین همان بی کربنات است؟
جوش شیرین فقط یک ماده تشکیل دهنده دارد. در واقع میشه گفت که جوش شیرین همان بی کربنات سدیم است. این ترکیب پایه ای است که در تماس با اسیدها مانند دوغ، ماست یا سرکه واکنش نشان می دهد. این واکنش دی اکسید کربن (CO2) را به صورت حباب مانند کف مایع تولید می کند. هنگام تهیه کالاهای پخته شده، این فرآیند “خمیرمایه شیمیایی” نامیده می شود، زیرا گاز CO2 به دام افتاده باعث خمیر می شود.
جوش شیرین خود “بی کربنات سدیم خالص” است. هنگامی که جوش شیرین با رطوبت و یک ماده اسیدی (به عنوان مثال ماست، شکلات، دوغ، عسل) ترکیب شود، در نتیجه واکنش شیمیایی حباب های دی اکسید کربن تولید می شود، که منبسط می شوند و باعث گسترش یا افزایش کالاهای پخته می شوند.
تولید جوش شیرین:
دو نوع فرآیند تولید برای سدیم هیدروژن کربنات وجود دارد: مرطوب و خشک.
به طور کلی، روش مورد استفاده برای تولید در مقیاس بزرگ، روش مرطوب است که در آن سدیم هیدروژن کربنات با تزریق گاز دی اکسید کربن در سود سوز آور حاصل از الکترولیز به عنوان کریستال رسوب می کند تا واکنش ایجاد کند.
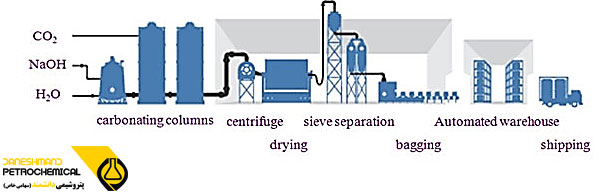
مراحل تولید بی کربنات سدیم به روش مرطوب:
1.آماده سازی: مقادیر کمیاب ناخالصی ها را در محلول ماده اولیه جدا کرده و از بین می برد. محلول فرآوری شده به مخزن ذخیره محلول تصفیه ارسال می شود.
- تبلور یا جداسازی: با تزریق گاز دی اکسید کربن، واکنشی ایجاد می شود که در آن بلورهای بی کربنات سدیم رسوب می کنند. از سانتریفیوژها برای جداسازی و حذف بلورها از محلول حاوی بلورهای بی کربنات سدیم استفاده کنید.
- خشک کردن یا الک کردن: پس از خشک شدن بی کربنات سدیم جدا شده، سپس با اندازه ذرات با استفاده از یک فرآیند الک ترتیب داده شده و به یک محصول تبدیل می شود.
جمع بندی
بی کربنات سدیم یا همان جوش شیرین، یک ترکیب شیمیایی چندمنظوره است که علاوه بر کاربرد گسترده در صنایع غذایی، دارویی، بهداشتی و شویندهها، نقش مهمی در خنثیسازی اسید و بهبود کیفیت محصولات دارد. این ماده با ویژگیهای خاص خود، از پخت و پز گرفته تا صنایع نساجی و تولید دارو، جایگاه ویژهای در زندگی روزمره و صنعت پیدا کرده است.
💬 نظر شما چیست؟
شما بیشتر جوش شیرین را در چه زمینهای استفاده کردهاید؟ در آشپزی، بهداشت شخصی یا صنعت؟
نظرتان را همین پایین با ما به اشتراک بگذارید 👇
لیست قیمت بی کربنات سدیم:
| ردیف | نام محصول | قیمت |
| 1 | قیمت جوش شیرین | تماس بگیرید |